Kako se proteini vezuju za specifične pratioce unutar ćelija
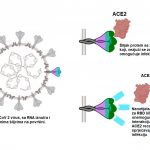
Uprkos svojoj maloj veličini, jedna ćelija sadrži milijarde molekula koji cirkulisu okolo i vezuju se jedni za druge, obavljajući vitalne funkcije. Ljudski genom kodira oko 20.000 proteina, od kojih većina stupa u interakciju sa partnerskim proteinima da bi posredovala u više od 400.000 različitih interakcija. Ovi partneri se ne vezuju samo slučajno jedan za drugog, vezuju se samo za vrlo specifične pratioce koje moraju prepoznati unutar prepune ćelije. Ako stvore pogrešne parove ili čak pravi parovi na pogrešnom mestu ili u pogrešno vreme, može doći do raka ili drugih bolesti. Naučnici naporno rade na istraživanju ovih između protein- protein odnosa , kako bi razumjeli kako oni funkcionišu i potencijalno kreirali lijekove koji ih ometaju ili oponašaju za liječenje bolesti.
Prosječan ljudski protein se sastoji od približno 400 građevnih blokova zvanih aminokiseline, koji su nanizani zajedno i presavijeni u složenu 3D strukturu. Unutar ovog dugačkog niza građevnih blokova, neki proteini sadrže delove od 4-6 aminokiselina koje se nazivaju kratkim linearnim motivima (short linear motifs -SLiMs), koji posreduju u protein-protein interakcijama. Uprkos svojoj jednostavnosti i maloj veličini, SLiM-ovi i njihovi vezujući partneri olakšavaju ključne ćelijske procese. Međutim, istorijski je bilo teško osmisliti eksperimente kako bi ispitali kako SLiM prepoznaju svoje specifične vezujuće partnere. Da bi se pozabavila ovim problemom, grupa koju je predvodila Tereza Hvang dizajnirala je metod skrininga kako bi razumjela kako se SLiM selektivno vezuju za određene proteine, pa čak i razlikuju one sa sličnim strukturama. Koristeći detaljne informacije koje su prikupili proučavanjem ovih interakcija, istraživači su stvorili sopstveni sintetički molekul sposoban da se izuzetno čvrsto veže za protein nazvan ENAH, koji je umiješan u metastaze raka. Da bi ispitali SLiM-ove sa širokim spektrom afiniteta vezivanja, Hvang i njihove kolege razvili su sopstveni ekran pod nazivom MassTitr.
Istraživači su takođe sumnjali da aminokiseline sa obje strane 4-6 aminokiselinske sekvence SLiM-a mogu igrati nedovoljno cijenjenu ulogu u vezivanju. Da bi testirali svoju teoriju, koristili su MassTitr za skrining ljudskog proteoma u dužim komadima koji se sastoje od 36 aminokiselina, kako bi vidjeli koji će se „prošireni“ SLiMs povezati sa proteinom ENAH.
ENAH, koji se ponekad naziva i Mena, pomaže ćelijama da se kreću. Naučnici su otkrili da smanjenje količine ENAH smanjuje sposobnost ćelija raka da napadnu druga tkiva, što sugeriše da bi formulisanje lijekova za poremećaj ovog proteina i njegovih interakcija moglo da liječi rak.
Zahvaljujući MassTitr-u, tim je identifikovao 33 proteina koji sadrže SLiM koji se vezuju za ENAH, od kojih su 19 potencijalno novi obavezujući partneri. Takođe su otkrili tri različita obrasca aminokiselina koje okružuju jezgro SLiM sekvence koje su pomogle SLiM-ima da se još čvršće vežu za ENAH. Od ovih proširenih SLiM-ova, jedan se nalazi u proteinu zvanom PCARE vezanom za ENAH sa najvećim poznatim afinitetom od bilo kog SLiM-a do sada.
Zatim su istraživači kombinovali kompjuterski program pod nazivom dTERMen sa rendgenskom kristalografijom kako bi razumeli kako i zašto se PCARE vezuje za ENAH preko ENAH-ova dva skoro identična sestrinska proteina (VASP i EVL). Hvang i njene kolege su videle da su aminokiseline koje okružuju PCARE jezgro SliM prouzrokovale da ENAH blago promijeni oblik kada su njih dvoje uspostavili kontakt, dozvoljavajući mestima vezivanja da se zakače jedno za drugo. VASP i EVL, nasuprot tome, nijesu mogli da pretrpe ovu strukturnu promjenu, tako da PCARE SliM nije bio tako čvrsto vezan ni za jednog od njih.
Inspirisana ovom jedinstvenom interakcijom, Hvang je dizajnirala sopstveni protein koji se vezuje za ENAH sa neviđenim afinitetom i specifičnošću. “Ovaj rad postavlja osnovu za dizajniranje sintetičkih molekula sa potencijalom da poremeti interakcije proteina i proteina koje izazivaju bolest – ili da pomogne naučnicima da saznaju više o ENAH i drugim SLiM-vezujućim proteinima”, kaže ona.
Ilva Ivarsson, profesor biohemije na Univerzitetu Upsala koja nije bila uključena u studiju, kaže da je razumijevanje načina na koji proteini pronalaze svoje vezujuće partnere pitanje od fundamentalnog značaja za funkciju i regulaciju ćelija. Studije eLife, objašnjava ona, pokazuju da prošireni SLiM-ovi igraju nedovoljno cijenjenu ulogu u određivanju afiniteta i specifičnosti ovih vezujućih interakcija.
„Studije su rasvetlile ideju da je kontekst bitan i daju strategiju skrininga za različite interakcije zavisne od konteksta“, kaže ona. “Hvang i koautori su stvorili vredne alate za seciranje ćelijske funkcije proteina i njihovih partnera za vezivanje. Njihov pristup bi čak mogao da inspiriše ENAH-specifične inhibitore u terapeutske svrhe.”
Najveći Hvangov zaključak iz projekta je da stvari nisu uvek onakve kakve izgledaju: čak i kratki, jednostavni segmenti proteina mogu igrati složene uloge u ćeliji. Kako ona kaže: „Trebalo bi da više cenimo SLiM-ove.“
Izvor:
news-medical.net
Reference:
Hwang, T., et al. (2022) Native proline-rich motifs exploit sequence context to target actin-remodeling Ena/VASP protein ENAH. eLife. doi.org/10.7554/eLife.70680.
https://naucnenovosti.me/kako-se-proteini-vezuju-za-specificne-pratioce-unutar-celija/https://naucnenovosti.me/wp-content/uploads/2022/02/photo-867159754-612x612-1.jpghttps://naucnenovosti.me/wp-content/uploads/2022/02/photo-867159754-612x612-1-150x150.jpgBiologijaNovostiproteiniUprkos svojoj maloj veličini, jedna ćelija sadrži milijarde molekula koji cirkulisu okolo i vezuju se jedni za druge, obavljajući vitalne funkcije. Ljudski genom kodira oko 20.000 proteina, od kojih većina stupa u interakciju sa partnerskim proteinima da bi posredovala u više od 400.000 različitih interakcija. Ovi partneri se ne...adminJovan Mirkovicjovan.mirkovic@prona.orgAdministratorNaučne Novosti